داروها چگونه طراحی و تولید می شوند؟

تولید داروی جدید فرآیندی پرهزینه و زمان بر است که مشمول مقررات گسترده ای است.
دارو چیست؟
داروها مواد شیمیایی یا بیولوژیکی هستند که ساختار فیزیولوژیک دارند؟ یا بیوشیمیایی؟ تاثیرشان روی بدن ما چگونه است
آنها ممکن است ترکیبات منفرد یا مخلوطی از ترکیبات مختلف باشند.
اثرات آنها سودمند است اما می تواند عوارض جانبی مضری در برخی افراد ایجاد کند.
- همه داروها با “هدف” خاص در بدن، با هدف اصلاح فعالیت خود که اغلب منجر به یک درمان در تعامل هستند. مثلاً اثر تسکین درد.
اهداف دارویی معمولا پروتئین هستند. اما آیا در برخی موارد مناطق کوچکی از DNA هستند؟ یا RNA؟
داروها با تحریک یا مسدود کردن فعالیت اهداف خود عمل می کنند.
چگونه یک دارو تولید می شود؟
توسعه یک داروی درمانی جدید یک فرآیند پیچیده، طولانی و پرهزینه است.
ممکن است 10 تا 15 سال طول بکشد و بیش از 500 میلیون پوند تولید یک دارو از یک مفهوم اولیه، آزمایش ایمنی و اثربخشی آن در انسان و سپس عرضه آن به بازار بیمارستان، شامل موارد زیر است:
2-4 سال توسعه پیش بالینی
3-6 سال توسعه بالینی
زمان اضافی برای تعامل با مقامات نظارتی.
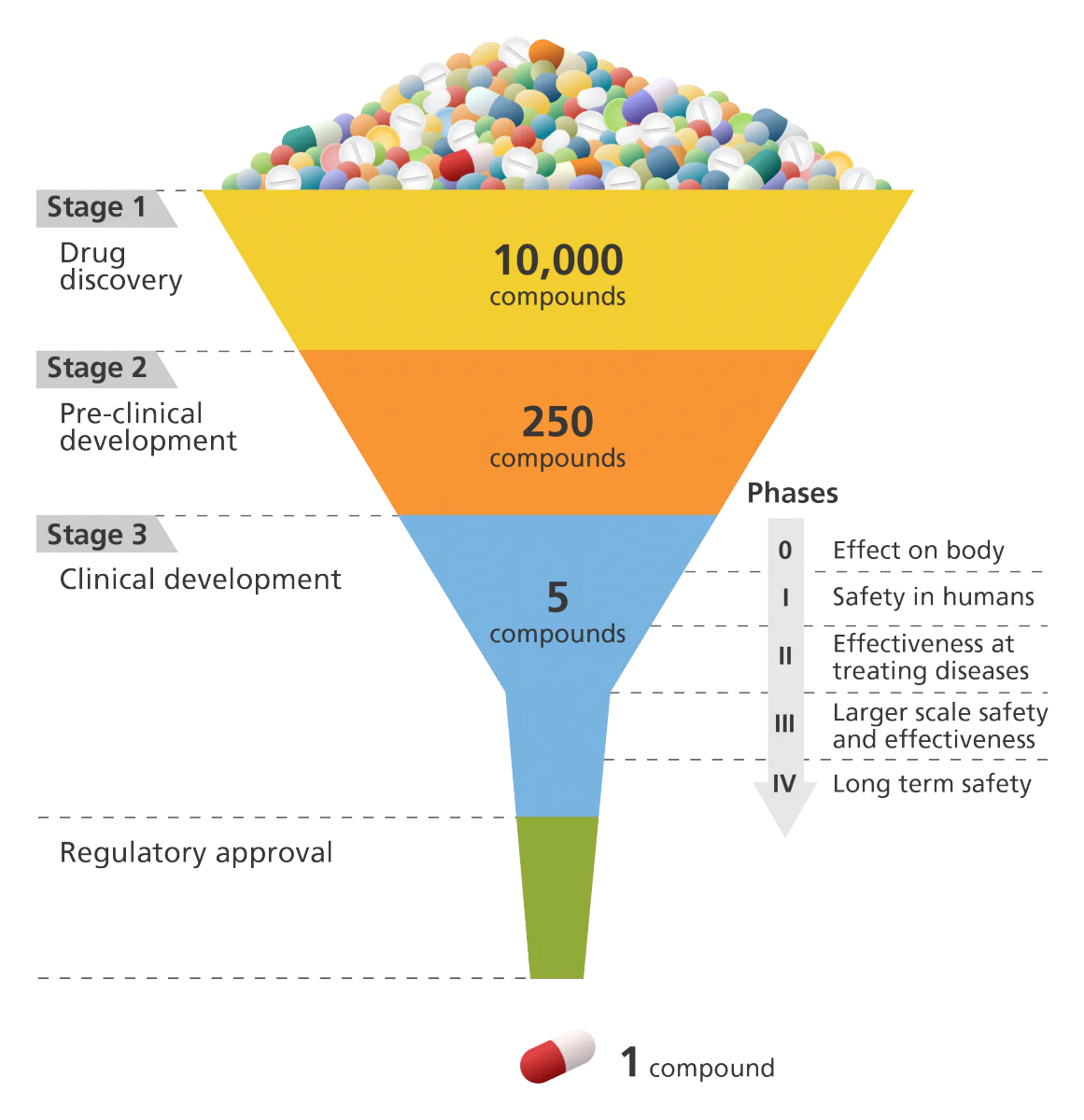
پله اول: کشف دارو
اولین مرحله از فرآیند تولید دارو، کشف دارو است.
در گذشته، برخی از داروها به طور تصادفی کشف شده اند، به عنوان مثال، پنی سیلین.
امروزه از رویکردهای سیستماتیک تری استفاده می شود، مانند:
غربالگری با توان عملیاتی بالا: که به دانشمندان اجازه می دهد هزاران هدف بالقوه را با هزاران ترکیب شیمیایی متنوع آزمایش کنند تا ترکیب دارویی-هدف جدیدی را شناسایی کنند.
طراحی منطقی دارو: که شامل طراحی و سنتز ترکیبات بر اساس ساختار شناخته شده یک مولکول هدف خاص است.در حالی که غربالگری با کارایی بالا ممکن است صدها جزء بالقوه سرب را شناسایی کند، بسیاری از آنها در اولین دور آزمایش حذف خواهند شد. در طی این دور ترکیبات در سلولها یا حیوانات کشتشده آزمایش میشوند تا مشخص شود که چقدر مؤثر هستند و آیا اثرات سمی دارند یا خیر.
طراحی منطقی دارو ترکیبات کمتری را در مقایسه با غربالگری با کارایی بالا ایجاد می کند. با این حال، این ترکیبات برای هدف بسیار خاص هستند و برای دستیابی به این ویژگی از مدل سازی مبتنی بر کامپیوتر استفاده می کنند.
پله دوم: توسعه پیش بالینی
- آزمایشات پیش بالینی برای تعیین بهترین روش تولید دارو برای استفاده مورد نظر انجام می شود.
هدف آن تعیین چگونگی جذب و توزیع داروها در بدن و نحوه تجزیه و حذف آنها از بدن است.
در صورت لزوم، داروهای امیدوارکننده ممکن است در تلاش برای بهبود خواص آنها به روشهای ظریف در فرآیندی به نام بهینهسازی سرب اصلاح شوند.
از نتایج آزمایشات پیش بالینی نیز برای تعیین بهترین فرمول دارو برای استفاده بالینی مورد نظر استفاده می شود، برای مثال اینکه آیا این دارو به عنوان کرم، قرص، تزریق یا اسپری موثرتر است.
هدف مطالعات پیش بالینی کاهش صدها ترکیب به تعداد چند داروی کاندید مفید است.
این چند دارو سپس به مقامات نظارتی مربوطه ارسال میشوند و در صورت پذیرش، ترکیب میتواند به توسعه بالینی منتقل شود.
پله سوم: توسعه بالینی
این به فازهای 0، I، II، III و IV تقسیم می شود.
توسعه بالینی که به عنوان آزمایشات بالینی نیز شناخته می شود، شامل آزمایش دارو بر روی داوطلبان انسانی برای ارائه اطلاعات بیشتر در مورد ایمنی و اثربخشی آن است.
تا پایان مرحله توسعه بالینی، اکثر داروهای جدید مورد بررسی به دلایل ایمنی و اثربخشی حذف خواهند شد.
- فقط یک یا دو ترکیب به عنوان یک درخواست دارویی جدید ارسال می شود. در بریتانیا، این به عنوان یک برنامه تاییدیه دارو شناخته می شود.
پس از تایید یک دارو توسط نهادهای نظارتی مربوطه، شرکت های داروسازی مدت کوتاهی دارند که در آن فقط آنها حق عرضه دارو را دارند (انحصار) و قبل از اینکه سایر شرکت ها بتوانند همان دارو را به بازار عرضه کنند.
این دوره انحصاری برای به دست آوردن مجدد سرمایه گذاری انبوه مورد نیاز برای توسعه و راه اندازی داروی جدید استفاده می شود.
پس از تایید کامل، شرکت های دارویی باید به آزمایش داروی خود ادامه دهند و بازخورد متخصصان مراقبت های بهداشتی را برای اطمینان از ایمنی و اثربخشی دارو نظارت کنند.
- پس از راه اندازی تولید یک دارو، ممکن است عوارض جانبی یا عوامل خطر جدیدی شناسایی شوند که قبلاً ثبت نشده بودند. این فاز IV توسعه بالینی است و بخشی از نظارت مداوم بر اثربخشی دارو در بیماران هدف آنها است.